Технические единицы измерения
Глава 2.1. Технические единицы измерения. В инженерно-технических отраслях промышленности используется много разных определений и единиц измерения, относящихся к механическим и тепловым свойствам веществ.
Это привело к появлению ряда проблем, для решения которых была создана согласованная международная система единиц измерения (от французского Systѐme International d’Unités), или система СИ. В этой системе имеется семь четко определённых единиц измерения, на основе которых определяются остальные единицы измерения, которыми мы и будем пользоваться в этой книге.
К основным единицам системы СИ относятся единицы длины (метр), массы (килограмм), времени (секунда) и температуры (Кельвин). Мы надеемся, что первые три в объяснении не нуждаются, а вот что такое Кельвин, мы позднее обсудим более подробно.
Кроме того, к основным единицам системы СИ относятся единица силы электрического тока (ампер), количества вещества (моль) и силы света (кандела). Эти единицы измерения могут быть знакомы читателю, разбирающемуся, соответственно, в электронике, химии и физике, но не имеющему отношение к паровой технике и не знающему, из чего состоит пароконденсатная система.
В таблице 2.1.1 перечислены производные единицы измерения, относящиеся к теме данной книги. Все они должны быть знакомы любому читателю с техническим образованием. Эти единицы измерения получили свои названия в честь знаменитых исследователей, внёсших свой вклад в развитие науки и техники.
Таблица 2.1.1 Производные единицы СИ, имеющие свои названия
| Измеряемая величина | Название | Символ | Основная единица СИ | Производная единица |
| Площадь | Квадратный метр | A | м2 | – |
| Объем | Кубический метр | V | м3 | – |
| Скорость | Метр в секунду | u | м/с | – |
| Ускорение | Метр в секунду в квадрате | a | м/с2 | – |
| Сила | Ньютон | N, H | кг м/с2 | Дж/м |
| Энергия | Джоуль | J, Дж | кг м2 / с2 | Н/м |
| Давление или нажим | Паскаль | Pa, Па | кг м/с2 | Н/м2 |
| Мощность | Ватт | W, Вт | кг м2/с3 | Дж/с |
Существует множество других производных единиц, полученных из основных единиц СИ и важных для того, кто имеет дело с паровой техникой. Эти единицы приведены в Таблице 2.1.2.
Таблица 2.1.2 Другие единицы измерения, выраженные в производных единицах СИ
| Измеряемая величина | Основная единица СИ | Производная единица |
| Массовая плотность | кг/м3 | кг/м3 |
| Удельный объем (Vg) | м3/кг | м3/кг |
| Удельная энтальпия (h) | м2/с2 | Дж/кг |
| Удельная теплоемкость (Cp) | м2/с2К | Дж/кг К |
| Удельная энтропия | м2/с2К | Дж/кг К |
| Интенсивность теплового потока | м2кг/с3 | Дж/с или Вт |
| Динамическая вязкость | кг/м с | Н м/м2 |
Обозначение с помощью точки
Такие обозначения используются для производных единиц измерения, в состав которых входит скорость изменения чего-либо, например:
m. = масса (например, в килограммах)
m = расход массы в единицу времени (например, кг/ч) = удельный массовый расход
Кратные и дольные приставки
В Таблице 2.1.3 приведён список приставок, используемых в названиях кратных и дольных единиц СИ. Эти приставки позволяют обходиться без очень больших и очень маленьких численных значений. Приставка «присоединяется» непосредственно к названию единицы измерения, а символ этой приставки – к символу, соответствующему этой единице измерения.
Например, одну тысяча метров можно обозначать как 1 км, 1000 м или 103м.
Таблица2.1.3Дольные и кратные приставки для единиц измерения СИ
| Кратные приставки | Кратные приставки | Кратные приставки | Дольные приставки | Дольные приставки | Дольные приставки |
| Множитель | Приставка | Обозначение | Множитель | Приставка | Обозначение |
| 1012 | Тера | Т | 10-3 | мили | м |
| 109 | Гига | Г | 10-6 | микро | мк |
| 106 | Мега | М | 10-9 | нано | н |
| 103 | Кило | К | 10-12 | пико | п |
Особые сокращения, используемые при измерении потока пара
По историческим причинам в Международном стандарте ISO 5167 (он заменил прежний стандарт BS 1042), описывающем правила измерения расходов, используются сокращения, приведённые в Таблице 2.1.4.
Таблица 2.1.4 Символы, используемые в измерении потоков
| Символ | Определение | Единица измерения |
| qm | Удельный расход масс | кг/с или кг/ч |
| qv | Удельный расход объема | м3/с |
| QL | Удельный расход жидкости | л/мин |
| Qs | Расход газа при нормальной температуре и давлении | л/мин |
| QF | Фактический расход газа | л/мин |
| QE | Эквивалентный удельный расход воды | л/мин |
| Ds | Плотность газа при нормальной температуре и давлении | кг/м3 |
| DF | Фактическая плотность газа | кг/м3 |
| Ps | Стандартное давление (1,013 бар абс.) | бар абс. |
| PF | Фактическое давление потока | бар абс. |
| Ts | Стандартная температура | ºС |
| TF | Фактическая температура потока | ºС |
Стандартная температура и давление
Это стандартные условия измерения свойств вещества. Стандартная температура – это температура замерзания чистой воды. Она составляет 0ºС, или 273,15ºК. Стандартное давление – это давление, создаваемое ртутным столбом (обозначается Hg) высотой 760 мм. Оно часто обозначается как 760 мм. рт. ст. Это давление также называют одной атмосферой, оно равно 1,01325 х 106 дин на квадратный сантиметр. Про плотность (масса на единицу объёма) газа обычно говорят, имея в виду значение плотности при стандартной температуре и давлении. Свойства, которые нельзя измерить при стандартной температуре и давлении, измеряются в других условиях. Полученные значения потом, как правило, математически экстраполируются, что позволяет получить соответствующие значения при нормальной температуре и давлении.
Символы
В таблице 2.1.5 приведены символы и типичные единицы измерения, используемые в описании пароконденсатной системы.
Таблица 2.1.5 Символы и единицы измерения, используемые при описании пароконденсатной системы
| Символ | Определение | Единица измерения |
| A | Площадь поперечного сечения проводника, в зависимости от условий работы | м2 или мм2 |
| cp | Удельная теплоемкость при постоянном давлении | кДж/кгºС или кДж/кг К |
| Cv | Удельная теплоемкость при постоянном объёме | кДж/м3ºС или кДж/ м3 К |
| D | Диаметр поперечного сечения круглого проводника | м или мм |
| d | Диаметр отверстия | м или мм |
| g | Ускорение свободного падения | 9,81 м/с2 |
| Hz | Единица измерения частоты (число циклов в секунду) | Гц или кГц |
| J | Джоуль, единица измерения энергии | Дж или кДж |
| L | Длина | м |
| M | Молярная масса жидкости | кг/моль |
| N | Ньютон, единица измерения силы | Н ли кН |
| Pa | Единица измерения давления (паскаль) | Па или кПа |
| p | Статическое давление жидкости | бар или кПа |
| Δp | Дифференциальное давление | бар или кПа |
| m | Фундаментальная единица измерения длины (метр) | м |
| m | Масса | кг |
| . m | Массовый расход | кг/с или кг/ч |
| ms | Массовый расход пара | кг/с или кг/ч |
| Q | Количество тепла | кДж |
| Q | Скорость переноса тепла | кДж/с (кВт) |
| R | Радиус | м или мм |
| ReD | Число Рейнольдса, относящееся к диаметру D | не имеет размерности |
| s | Фундаментальная единица измерения времени (секунда) | сек |
| Sr | Число Струхаля | не имеет размерности |
| σ | Напряжение | Н/м2 |
| Тs | Температура пара | К или ºС |
| TL | Температура жидкости (или вещества) | К или ºС |
| ΔT | Разность температур или изменение температуры | К или ºС |
| t | Время | с или ч |
| u | Скорость движения жидкости | м/с |
| μ | Динамическая вязкость жидкости | Па с или сР |
| ν | Кинематическая вязкость | сСт |
| ρ | Плотность жидкости | кг/м3 |
| V• | Удельный объёмный расход | м3/с или м3/ч |
| W | Единица измерения потока энергии (Ватт) | Вт (Дж/с) |
| V (vg) | Объем (удельный объём) | м3 (м3/кг) |
| H (hg) | Энтальпия (удельная энтальпия) | кДж (кДж/кг) |
| S (sg) | Энтропия (удельная энтропия) | кДж К (кДж/кг К) |
| U (ug) | Внутренняя энергия (удельная внутренняя энергия) | кДж (кДж/кг) |
Нижние индексы, используемые для определения свойств веществ
Когда говорят об энтальпии, энтропии и внутренней энергии, то для указания фазы используют описанные далее нижние индексы:
Нижний индекс f означает жидкость или жидкое состояние. Например, hf – энтальпия жидкости.
Нижний индекс fg означает переход из жидкого состояния в газообразное. Например, hfg – энтальпия испарения.
Нижний индекс g означает общий показатель. Например, hg – общая энтальпия.
Обратите внимание на то, что, по умолчанию, общее количество тепла в перегретом паре обозначается символом h.
Кроме того, по умолчанию общие величины чаще всего обозначают прописными буквами, а удельные величины – строчными.
Например:
Общая энтальпия пробы перегретого пара: H кДж
Удельная энтальпия перегретого пара: h кДж/кг
Температура
Температурная шкала используется в качестве индикатора теплового равновесия, в том смысле, что любые контактирующие друг с другом тепловые системы, температуры в которых одинаковы, находятся в тепловом равновесии.
Шкала цельсия (ºС)
Этой шкалой инженеры пользуются чаще всего. Она отличается очень удобным значением нулевой температуры, соответствующим температуре, при которой замерзает вода.
Абсолютная шкала или шкала Кельвина (К)
Инкремент этой шкалы такой же, как и шкалы Цельсия, однако нулевое значение соответствует минимальной возможной температуре, при которой движение всех молекул и атомов прекращается. Эту температуру часто называют абсолютным нулем (0 К); она равна –273,15ºС.
Эти две температурные шкалы взаимозаменяемы, что показано на Рисунке 2.1.1. Ниже приведено уравнение, описывающее связь между шкалами Кельвина и Цельсия.
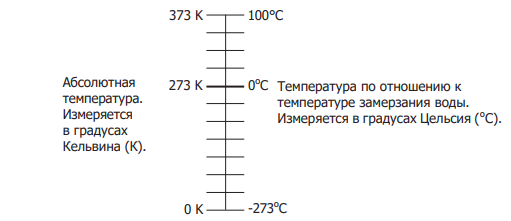
Рисунок 2.1.1 Сравнение абсолютной и относительной температуры

В системе СИ единицей измерения температуры является кельвин. Он определён как 1 ÷ 273,15 термодинамической температуры чистой воды в ее тройной точке (0,01ºС). О том, что такое тройная точка, вы можете прочитать в Главе 2.2.
В большинстве уравнений термодинамики температуру нужно записывать в кельвинах. Однако разность температур, часто используемую при вычислении параметров теплопереноса, можно выражать как в градусах Цельсия, так и в кельвинах. Поскольку инкремент обеих шкал одинаков, разность температур, равная 1º, соответствует разности температур, равной 1 К.
Давление
В качестве единицы измерения давления в системе СИ принят паскаль (Па), определяемый как сила, равная 1 Ньютону, действующая на площадь в один квадратный метр (1 Н/м2). Поскольку один паскаль соответствует очень малому давлению, в паровой технике обычно используются такие единицы, как килопаскаль (кПа, 1 кН/м2) или мегапаскаль (МПа, 1 МН/м2).
Однако наиболее часто используемой в паровой технике метрической единицей для измерения давления является бар. Один бар равен 105 Н/м2 и примерно равен одной атмосфере. В настоящем издании мы пользуемся именно этой единицей измерения.
К другим часто используемым единицам измерения давления относятся фунт на квадратный дюйм (psi, фунт на квадратный дюйм), кг/см2, атм., миллиметр водяного столба и миллиметр ртутного столба. Коэффициенты преобразования одних единиц в другие вы легко можете найти в самых разных источниках.
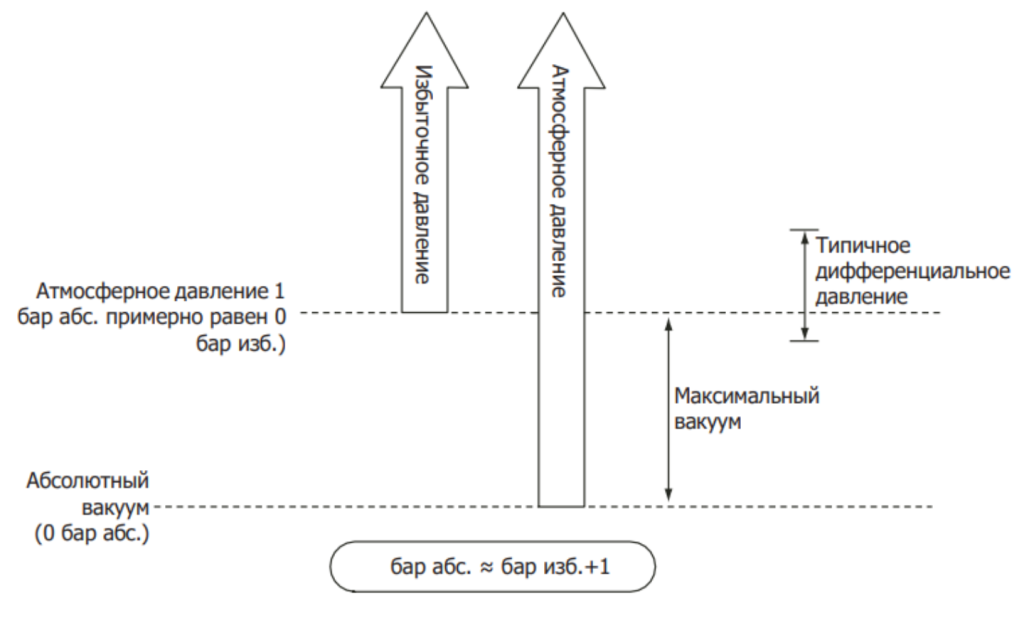
Рисунок 2.1.2 Сравнение абсолютного и избыточного давления
Абсолютное давление (бар абс. или бара)
Абсолютное давление – это давление, измеренное по сравнению с абсолютным вакуумом. Давление абсолютного вакуума составляет 0 бар абс.
Избыточное давление (бар изб. или бари)
Избыточное давление – это давление, измеренное по сравнению с атмосферным давлением. Хотя в реальной жизни атмосферное давление зависит от климатических условий и высоты над уровнем моря, в качестве атмосферного давления часто используют значение, равное 1,01325 бар абс. (1 атм). Оно представляет собой давление, оказываемое воздухом атмосферы Земли на уровне моря.
Избыточное давление = абсолютное давление – атмосферное давление
Если давление выше атмосферного, оно всегда соответствует положительному избыточному давлению. И наоборот, вакуум, или отрицательное давление, – это давление ниже атмосферного. Давление, равное –1 бар изб., практически соответствует абсолютному вакууму.
Дифференциальное давление
Дифференциальное давление – это разница между двумя давлениями. При определении дифференциального давления не нужно использовать обозначения «изб.» и «абс.» для обозначения, соответственно, избыточного и абсолютного давления, поскольку базовые значения давления в таком случае не важны.
Поэтому разница между двумя давлениями будет одинаковой вне зависимости от того, какое давление при этом измерялось – относительное или абсолютное. Главное, чтобы оба значения давления измерялись относительно одного и того же базового значения.
Плотность и удельный объем
Плотность вещества (ρ) можно определить как массу этого вещества (m), деленную на занимаемый им объем (V). Удельный объем (vg) – это объем единицы массы, то есть величина, обратная плотности. Фактически, термин «удельный» обычно используется для обозначения свойства единицы массы вещества (см. Уравнение 2.1.2).
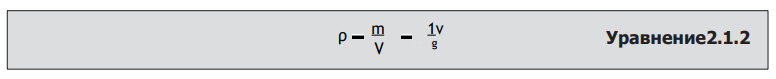
Где:
ρ = Плотность (кг/м3)
m = Масса (кг)
V = Объем (м3)
vg = Удельный объем (м3/кг)
Единицей измерения плотности в СИ является кг/м3, а единицей удельного объема, наоборот, является м3/кг.
В качестве меры плотности используется также удельный вес. Он представляет собой соотношение плотности вещества (ρs) и плотности чистой воды (ρw) при нормальной температуре и давлении (STP).
Этим стандартным условиям обычно соответствует атмосферное давление и температура 0ºС. Иногда стандартным условием считают температуру 20ºС или 25ºС. Такие условия называют нормальной температурой и давлением (НТД).

Плотность воды при этих условиях составляет примерно 1000 кг/м3. Поэтому вещества, обладающие плотностью, превышающей это значение, имеют удельный вес больше 1, тогда как вещества, обладающие меньшей плотностью, имеют удельный вес меньше 1.
Поскольку удельный вес – это соотношение между двумя плотностями, он не имеет размерности и единицы измерения. Таким образом, термин «удельный» не означает, что это свойство соответствует единичной массе вещества. Удельный вес также иногда называют относительной плотностью вещества.
Теплота, работа и энергия
Энергию иногда определяют как способность совершать работу. Передача энергии путем механического движения называется работой. Единица измерения работы и энергии в СИ – джоуль, который равен 1 Нм.
Количество выполняемой механической работы можно определить при помощи уравнения, полученного из ньютоновской механики:
Работа = сила х перемещение
Работу можно также определить как произведение давления на вытесненный объем:
Работа = давление х вытесненный объем
Пример 2.1.1
Давление 1 Па (или 1 Н/м2) вытесняет объем 1 м3. Какая работа при этом совершается?
Совершенная работа = 1 Н/м2 х 1 м3 = 1 Н м (или 1 Дж)
Преимущество использования единиц СИ (как в приведённом выше примере) состоит в том, что они в уравнении, по сути дела, взаимно уничтожаются, и в результате получается искомая единица измерения.
Проведённые Дж. П. Джоулем эксперименты и наблюдения показали, что механическая энергия (или работа) и теплота эквивалентны. Он установил, что для одного и того же увеличения температуры удельной массы воды требуется одинаковое количество энергии, вне зависимости от того, каким образом передавалась воде энергия – посредством работы или передачи тепла.
Полная энергия системы состоит из внутренней, потенциальной и кинетической энергии. Температура вещества непосредственно связана с его внутренней энергией (ug). Внутренняя энергия связана с движением и взаимодействием составляющих это вещество молекул, а также с молекулярными связями этого вещества. Внешняя энергия вещества связана с его скоростью и расположением и представляет собой сумму кинетической и потенциальной энергии.
Перенос энергии только в результате разницы температур называют тепловым потоком. Ватт, который является единицей измерения мощности в СИ, можно определить как тепловой поток, равный 1 Дж/с.
Кроме того, для измерения тепловой энергии используются британские тепловые единицы (БТЕ, количество теплоты, позволяющее нагреть 1 фунт воды на 1ºF) и килокаллории (количество теплоты, позволяющее нагреть 1 кг воды на 1ºС). Коэффициенты преобразования одних единиц в другие вы легко можете найти в самых разных источниках.
Удельная энтальпия
Термином «энтальпия» обозначается полная, определяемая давлением и температурой энергия текучей среды (воды или пара) в любом состоянии в любой данный момент времени. Говоря конкретнее, энтальпия – это сумма внутренней энергии и работы, производимой при данном давлении (как в примере 2.1.1).
Основной единицей измерения энтальпии является джоуль (Дж). Поскольку один джоуль соответствует очень малому количеству энергии, обычно пользуются килоджоулем (кДж), равным 1000 джоулей.
Удельная энтальпия – это мера полной энергии единичной массы, а в качестве единицы ее измерения обычно используют кДж/кг.
Удельная теплоемкость
Энтальпия текучей среды является функцией температуры и давления этой среды. Зависимость энтальпии от температуры можно определить, измерив повышение температуры, вызываемое тепловым потоком при постоянном давлении. Теплоемкость при постоянном давлении, ср, – это мера изменения энтальпии при определённой температуре.
Точно так же, внутренняя энергия является функцией температуры при определённом объёме. Теплоемкость при постоянном объёме, сv, – это мера изменения внутренней энергии при определённой температуре и постоянном объёме.
Поскольку удельный объем твёрдых и жидких материалов обычно меньше, то работой, производимой давлением, можно пренебречь, за исключением случаев, когда давление очень велико. Поэтому, если энтальпию представить только как внутреннюю энергию, можно будет сказать, что удельная тепло- емкость при постоянном объёме равна теплоемкости при постоянном давлении.
Таким образом, для твёрдых и жидких материалов: ср ≈ cv
Другое упрощение, касающееся твёрдых и жидких материалов, учитывает их несжимаемость, и заключается в том, что объем таких веществ является функцией одной лишь температуры. Из этого следует, что энтальпия и теплоемкость несжимаемой жидкости также являются функциями одной лишь температуры.
Удельная теплоемкость представляет собой количество энергии, необходимое для нагрева 1 кг вещества на 1ºС. Ее также можно рассматривать как способность вещества поглощать тепло. Поэтому единицей измерения удельной теплоемкости в системе СИ является кДж/кг К (кДж/кгºС). По сравнению со многими другими жидкостями вода обладает большой удельной теплоемкостью (4,19 кДж/кгºС). Поэтому воду и пар можно считать хорошими переносчиками тепла.
Количество тепловой энергии, необходимое для повышения температуры вещества, можно определить при помощи уравнения 2.1.4.

Где:
Q = Количество энергии (кДж)
m = Масса вещества (кг)
ср = Удельная теплоемкость вещества (кДж/кгºС) ΔT = Повышение температуры вещества (ºС)
Это уравнение показывает, что для данной массы вещества повышение температуры линейно связано с количеством подаваемого тепла, при условии, что удельная теплоемкость в данном диапазоне температур остаётся постоянной.
Пример 2.1.2
Имеется 2 литра воды, температура которой увеличивается с 20ºС до 70ºС.
При атмосферном давлении плотность воды составляет примерно 1000 кг/м3. Так как в одном кубическом метре находится 1000 литров, плотность можно выразить как 1 кг на литр (1 кг/л). Поэтому масса воды составляет 2 кг.
Удельная теплоемкость воды при небольших температурах составляет 4,19 кДж/кгºС. Поэтому: Q = 2 кг х 4,19 кДж/кгºС х (70 – 20)ºС = 419 кДж
Охлаждение воды до исходных 20°C освобождает ранее накопленную энергию выше.
Энтропия (S)
Энтропия – это мера беспорядка в системе. Чем выше степень беспорядка, тем выше энтропия. В системе СИ в качестве единицы измерения энтропии принят кДж/кг К (кДж/кгºС).
В твёрдых веществах молекулы располагаются сами, создавая упорядоченную структуру. Когда вещество переходит из твёрдого состояния в жидкое или из жидкого в газообразное, расположение молекул становится менее упорядоченным, и они начинают двигаться более свободно. Энтропия любого вещества в газообразном состоянии выше, чем энтропия этого же вещества в жидком состоянии, а энтропия жидкого вещества выше, чем энтропия этого же вещества в твёрдом состоянии.
Одной из характеристик всех естественных и спонтанных процессов является то, что все они направлены на достижение состояния равновесия.
Это свойство отражено во втором законе термодинамики, который гласит, что тепло не может переходить от более холодного тела к более теплому.
Изменение энтропии системы вызывается изменением содержащейся в ней тепла, причем изменение энтропии равно изменению количества тепла, деленному на среднюю абсолютную температуру. (Уравнение 2.1.5).

Когда вычисления проводятся для единичной массы, символы энтропии и энтальпии записываются в нижнем регистре. (Уравнение 2.1.6).

Для того чтобы проиллюстрировать это более подробно, рассмотрим следующие примеры:
Пример 2.1.3
В ходе процесса 1 кг воды нагревается от 0 до 100ºС (от 273 до 373 К) в нормальных атмосферных условиях.
Удельная энтальпия при температуре 0ºС = 0 кДж/кг (из таблиц водяного пара)
Удельная энтальпия воды при температуре 100С = 419 кДж/кг (из таблиц водяного пара)
Вычислим изменение удельной энтропии
Поскольку мы имеем дело с изменением удельной энтропии воды, к символу «s» в Уравнении 2.1.6
добавляется нижний индекс «f»: sf.

Пример 2.1.4
В ходе процесса 1 кг воды, имеющей температуру 100ºС (373 К) в нормальных атмосферных условиях превращается в насыщенный пар, имеющий ту же температуру 100ºС (373 К).
Вычислим изменение удельной энтропии при испарении
Поскольку мы имеем дело с изменением удельной энтропии при изменении состояния вещества, к
символу «s» в Уравнении 2.1.6 добавляется нижний индекс «g»: Sg.
Удельная энтальпия испарения
пара при температуре 100ºС (373 К) (hfg) = 2258 кДж/кг (из таблиц водяного пара)
Удельная энтальпия испарения
воды при температуре 100ºС (373 К) (hfg) = 0 кДж/кг (из таблиц водяного пара)
Вычисление:

Общее изменение удельной энтропии при превращении воды, имеющей температуру 0ºС, в насыщенный пар, имеющий температуру 100ºС, равно сумме удельной энтропии воды и изменения удельной энтропии пара. Для обозначения общего изменения удельной энтропии используется нижний индекс «g»: sg.
Таким образом:

Пример 2.1.5
В ходе процесса 1 кг насыщенного пара при атмосферном давлении перегревается до температуры 150ºС (423 К). Определим изменение энтропии.
Полная удельная энтальпия пара при атмосферном давлении
и температуре 100ºС (373 К) (hg) = 2675 кДж/кг (из таблиц водяного пара)
Полная удельная энтальпия пара при атмосферном давлении
и температуре 150ºС (423 К) (h) = 2777 кДж/кг (из таблиц водяного пара)
Изменение удельной энтальпии (Δh) = 102 кДж/кг

Средняя абсолютная температура=398К

Изменение удельной энтропии (Δs)=0,256 кДж/К
Полное изменение удельной энтропии (Δs) = Δsg +дополнительная энтропия, связанная с перегревом (Δs)
Полное изменение удельной энтропии = 7,351 кДж/кг К (из Уравнения 2.1.4 + 0,256 кДж/кг К)
изменение удельной энтропии =7,607 кДж/кгК
Поскольку энтропия насыщенной воды измеряется от условного значения 0,01ºС, энтропию воды при температуре 0ºС из практических соображений можно считать равным нулю. Полное изменение удельной энтропии в данном примере основано на первоначальной температуре воды 0ºС, поэтому конечный результат практически совпадает с удельной энтропией пара, которую можно найти в таблицах водяного пара для окончательного состояния пара при атмосферном давлении и температуре 150ºС.
Энтропия обсуждается более подробно в Главах 2.15 и 2.16.
Читать статьи о паре: О паре – ООО “НОСТ-СОЛЮШЕНС”
Читать статьи на Яндекс.Дзен: Nost Solutions | Дзен

